機體局部組織或細胞死亡後經一系列酶作用後,發生的形態學改變。壞死可局限於一個細胞,可大到一個器官的大部分或肢體的一部分。在形態上壞死的細胞主要表現為細胞核濃縮、核碎裂及核溶解消失。胞漿在蘇木素-伊紅染色片中為紅色(稱嗜酸性變),最後胞膜破裂,細胞消失。實際上細胞在最早壞死時,形態上並無明顯的改變,但是代謝已經停止,原有功能已經喪失。之後,進一步的改變是細胞內的膜系統破壞,主要是溶酶體釋放出大量各種水解酶,作用於細胞本身的結果。如皮下膿腫時皮下組織的壞死液化化,四氯化碳中毒時的肝細胞壞死,結核病時的幹酪樣壞死,腦血流中斷時的腦壞死(腦軟化)等。壞死也是炎癥的基本病理變化(變質)的一部分,壞死多由變性發展而來,少數情況下由於強烈的致病因子迅速致成。組織和細胞壞死後即喪失其功能。因此,重要器官的范圍較大的壞死如心肌梗死或重度病毒性肝炎肝壞死可招致機體死亡。次要部位的小范圍壞死則影響較小。壞死的組織對機體成為異物,可被機體清除,留下的缺損由鄰近健康組織再生修復。壞死組織的結局有溶解吸收(范圍小者)和分離排出(范圍大者)。壞死組織與健康組織分離脫落,在皮膚粘膜則形成潰瘍,在肺、腎等的幹酪樣壞死灶則形成空洞、機化(壞死組織范圍大、不能完全溶解、吸收或脫落排出,新生毛細血管及成纖維細胞從周圍長入,形成肉芽組織,最後形成瘢痕,取代壞死組織)或被包裹、鈣化。
壞死的機理 致病因子種類繁多,引起壞死的機理並非完全相同,但有如下的基本環節:①細胞的膜結構受損害。②線粒體功能障礙,ATP合成減少,這兩種損害往往同時發生並相互影響。
細胞的膜系統含磷脂及蛋白質,若細胞內Ca2+濃度增高,則激活磷脂酶A及B,這些酶作用於膜磷脂,使分解出脂肪酸,致膜系統遭損害。有時脂質的降解產物(如缺氧時產生的酰基肉堿與溶血磷脂質)堆積,由於ATP減少膜蛋白磷酸化作用降低,膜磷脂合成減少,由於缺氧細胞釋放自由基,這些均可損害細胞的膜結構。
細胞內的溶酶體由膜包繞,若膜受損則溶酶體所含的酶如核糖核酸酶、脫氧核糖核酸酶、蛋白酶、磷酸酶、葡糖苷酶等被釋出,這些酶在細胞內pH降低(因ATP減少)時被激活作用於核蛋白,使核蛋白降解為核酸、核苷酸、核苷及磷酸等,核則遭破壞而呈強嗜堿性,形態上則表現為上述的核濃縮、核碎裂和核溶解。
線粒體也由膜包繞,若膜受損則Ca2+大量進入線粒體,蛋白質變質,抑制酶活性,線粒體內氧化磷酸化功能遭破壞,ATP合成難以進行,因此ATP減少(一分子葡萄糖經無氧糖酵解僅可產生兩個ATP,若經線粒體內氧化磷酸化可產生36個ATP)。因此細胞能源缺乏,生命活動難以維持正常。
壞死的種類 一般分為凝固性及液化性壞死兩類。前者其特征是壞死的細胞呈嗜酸性,核已不著色,但仍保存其細胞輪廓及組織結構的圖像,常見於組織急劇血流中斷(如腎、脾的梗死)、中毒(如氯化汞中毒)、結核病幹酪樣壞死等時,產生機理可能是溶酶體酶遭破壞或沒有足夠的時間發揮作用。凝固性壞死在數日後,亦可慢慢發生液化,並為吞噬細胞吞噬、清除。後者多因壞死的細胞或組織蛋白質被主要來自白細胞的大量水解酶作用,致細菌或組織液化,失去原有的輪廓及結構,常見於化膿性細菌感染,這時壞死的組織和白細胞一起形成膿液。腦缺血時也會發生液化性壞死(稱腦軟化),這可能與腦組織含脂質豐富有關。
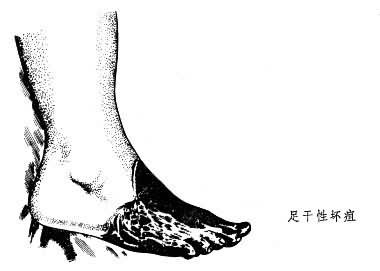
另外還有一些特殊形式的壞死,如:①壞疽性壞死,常見於肢體或腸的一部分,由於血流中斷如血栓閉塞性脈管炎或血栓形成時,壞死後有細菌侵入(如產氣莢膜桿菌、梭形桿菌等),破壞蛋白質(產生硫化氫)和紅細胞(產生Fe2+),形成硫化鐵(Fe2S3),致壞死部分呈黑色,並有腐敗氣味。若發生於四肢末端,則壞死部幹燥,稱幹性壞疽(見圖);若發生於腸,則壞死組織濕潤,稱濕性壞疽。氣性壞疽是濕性壞疽的一個特稱類型,壞死組織呈蜂窩狀、中含氣泡,污穢而呈暗棕色,觸之有捻發感,惡臭,為深達肌肉的開放性創傷組織合並產氣莢膜桿菌等感染所致。②新生兒皮下壞死,見於難產或產鉗助產的新生兒,身體受壓部位(背部和臀部)皮膚變硬,紅腫,中心軟化逐漸壞死,可融合成大片壞疽。③幹酪樣壞死,主要見於結核病灶,淡黃性、易碎,狀如幹酪,故名。因結核桿菌的膜中含有脂多糖所致,其致壞死的機理尚不清楚。④酶性脂肪壞死。如急性胰腺壞死。胰腺體或導管被破壞時,胰脂肪酶得以逸出,由於膽汁逆流等因素而被激活,與脂肪組織胰組織接觸,引起壞死。若與腹腔內組織接觸,可引起腹腔組織壞死,壞死的脂肪組織產生脂肪酸及甘油,脂肪酸與鈣離子結合形成鈣皂(鈣鹽)沉著於壞死組織中。若血管遭破壞,則有出血。⑤纖維素樣壞死,主要見於免疫性損傷,例如急性風濕病時,心臟二尖瓣瓣膜上可產生局灶的膠原纖維變性崩解伴有血漿纖維蛋白和球蛋白的沉積,蘇木素-伊紅染色呈深紅色,呈纖維素樣故稱纖維素樣壞死。在惡性高血壓病時的小動脈壁,同樣可見到血漿蛋白滲入,及血管壁的纖維素樣壞死。