末梢支氣管遠端氣腔的異常增大,伴有相應組織結構破壞者,稱為肺氣腫。若僅是單純的氣腔充氣則稱為肺過度充氣。肺氣腫常繼發於慢性阻塞性支氣管炎後(見慢性支氣管炎)或原發於慢性支氣管刺激物(如吸煙和有毒的物理化學因素)的長期作用,導致肺組織的器質性破壞,或併發慢性支氣管炎,與慢支互為因果。實屬慢性阻塞性肺疾病(COPD)病程中的一個階段,故稱“阻塞性肺氣腫”。最終導致肺功能不全和肺心病,危害性極大。在中國,90%的慢性肺源性心臟病的病因是慢支和阻塞性肺氣腫。
病因和病理 肺氣腫的發病機理尚未闡明,重要的致病因素有兩方面:
① 吸煙、大氣污染和炎癥感染,這些因素在肺氣腫發病中占有重要地位,尤以吸煙為甚。吸煙可致小氣道急、慢性炎癥,引起中性粒細胞和肺泡巨噬細胞增多。組織內浸潤的細胞死亡後釋放出各種蛋白酶,使蛋白酶──抗蛋白酶系統的平衡受到破壞,其中以中性粒細胞的作用最為顯著,因組織內中性粒細胞的壽命僅數小時,並釋放出大量彈力蛋白酶,必然導致肺氣腫。此外,支氣管系統的長期炎癥反應促使粘液分泌過多,纖毛上皮細胞的防禦機制削弱和破壞、上皮細胞的脫落及小氣道周圍結締組織的纖維化等病理改變,使氣道發生狹窄和呼吸氣流受阻,加速阻塞性肺氣腫的形成。
② 遺傳素質,某些先天遺傳性結締組織疾病,如嬰兒皮膚松弛癥和馬爾方氏綜合征,常並發肺氣腫。此外,α1-抗胰蛋白酶(α1AT)缺乏癥和肺氣腫的發生有密切關系。α1AT是由肝臟分泌的一種糖蛋白,可以抑制多種蛋白酶的活性,而對彈力蛋白酶的抑制作用更強。抑制蛋白酶的活力,90%存在於α1球蛋白內。其在血清內的含量或活力受染色體隱性基因的控制,因此是一種遺傳性疾病。在美國這種肺氣腫約占慢性阻塞性肺疾病的0.5~2%,而黑人中則幾乎接近零,表明瞭顯著的種族差異。此類患者中40歲以前發病者占60%,而50歲以前發病者高達90%。患者體內α1AT含量和抑制蛋白酶的活力很低,體內的蛋白酶-抗蛋白酶系統的正常平衡被破壞,使肺組織內彈力蛋白酶的活力增加,其對蛋白的消化作用損傷肺組織而形成肺氣腫。中國至今尚未發現這類患者。
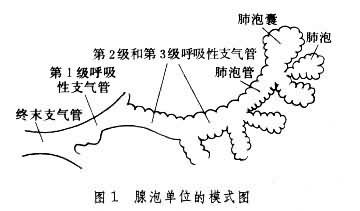
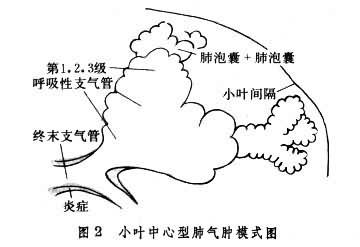
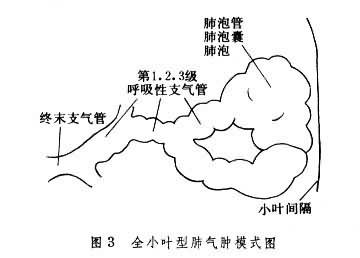
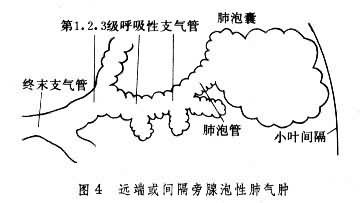
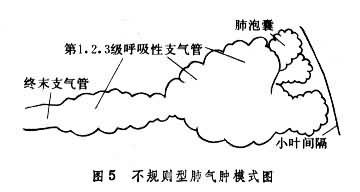
肺氣腫的主要病理改變在肺的腺泡單位。腺泡是指終末支氣管以下的三級呼吸性支氣管及所屬的肺泡管、肺泡囊和肺泡 (圖1)。每根終末支氣管支配著相應的腺泡單位,而每3~5根終末支氣管則組成一個次級小葉(或稱肺細葉)。根據小葉內受累腺泡的不同部位和數量,從病理學上將肺氣腫分為四型:①小葉中心型或腺泡中心型肺氣腫,又稱腺泡近端型肺氣腫,氣腫區位於次級小葉的中央(腺泡的近端)主要是呼吸性支氣管明顯擴大和組織結構的破壞,並有明顯炎癥反應 (圖2)。受累的腺泡氣腫區之間肺組織正常。遠端肺泡可無病理改變,此型肺氣腫多見於慢性支氣管炎。此外,還有一種局灶型肺氣腫,其病變部位與小葉中心型相似,位於腺泡的近端。不同處為氣腫區比較散在,周圍有明顯煤塵顆粒沉著,呼吸性支氣管隻有中等度擴大,肺功能損害較輕,多見於煤礦工人的單純塵肺。②全腺泡(小葉)型肺氣腫,氣腫區可遍及整個腺泡(圖3)。肺容積增大,其切面可見腺泡組織嚴重破壞,有許多增大的氣腫區,肺下葉受累程度較重。此型肺氣腫多見於α1-抗胰蛋白酶缺乏癥。也可見於重度急性支氣管或細支氣管炎引起的一側肺氣腫,即麥克勞德氏綜合征。此外小葉中心型肺氣腫也可發展為全小葉型。③遠端或間隔旁肺氣腫,氣腫區主要累及鄰近小葉間隔或臟層胸膜面的肺泡囊(圖4),伴有明顯纖維化改變。增大的肺泡囊在臟層胸膜下形成氣腫小泡,常是年輕人自發性氣胸的病理基礎。此型肺氣腫多見於上葉前、後側面,偶見下葉後面,也可和其他類型肺氣腫同時存在。其病因至今不明。④瘢痕旁或不規則肺氣腫,氣腫區與肺瘢痕組織緊密相鄰,氣腫區在小葉內呈不規則的散在分佈(圖5),組織切片可見和氣腫區鄰近的瘢痕組織內彈力蛋白組織著色區,其間有多數萎陷的肺泡。此型肺氣腫常見於工業性塵肺,如矽肺或肺內炎癥遲緩吸收和機化形成瘢痕後。
臨床表現與診斷 輕癥可無癥狀與體征。重癥時有氣短、呼吸困難,活動後加重,伴咳嗽、咯痰。體檢可見胸廓前後徑增大呈桶狀,叩診呈過清音甚至鼓音,呼吸音低,呼氣時更明顯。若合並肺心病則有相應的心力衰竭和肺功能不全的臨床表現。診斷應根據病史、體檢、X 射線檢查、心電圖、肺功能(如殘氣量增加,第一秒用力呼氣量明顯降低,第一秒用力呼氣量占用力肺活量百分數也降低)(見慢性支氣管炎)等實驗室檢查和相應的化驗檢查的結果,做出病因診斷。
防治 避免病原因素的接觸、加強環境衛生、禁止吸煙、進行體育鍛煉增強體質等都具有效的預防措施。治療重點在於控制感染、祛痰和平喘。低氧血癥患者應予以氧療,進行腹式呼吸鍛煉。