運用量子力學的理論、概念和方法研究生命物質和生命過程的一門學科,又稱量子生物物理學。量子力學的創立和發展,吸引著物理學傢和化學傢,促使他們用以分析具有生物學意義的分子之電子結構,並把結果和生物學活性聯繫起來。例如,1938年R.F.施密特就已開始對致癌芳香烴類化合物進行研究,試圖說明致癌活性與分子的電子結構之間的關係。以後經過普爾曼等人的工作,現已成為量子生物學的一個重要組成部分。
1930年物理學傢P.約爾丹進一步提出出瞭“突變是一種量子過程”,這一觀點在1944年E.薛定諤的《生命是什麼》一書中得到瞭詳盡的闡述。他還提出瞭遺傳物質是一種有機分子,遺傳性狀以“密碼”形式通過染色體而傳遞等設想。這些設想由於J.D.沃森與F.H.C.克裡克提出脫氧核糖核酸雙螺旋結構模型而得到極大的發展,從而奠定瞭分子生物學的基礎。分子的相互作用必然涉及其外圍電子的行為,而能夠精確描述電子行為的手段就是量子力學。因此量子生物學是分子生物學深入發展的必然趨勢,是量子力學與分子生物學發展到一定階段之後相互結合的產物。
研究方法 基本上就是用量子力學的方法來處理一個微觀體系的全部計算過程,並利用由此得出的各種參量,說明所研究對象的結構、能量狀態及變化,進而解釋其生物學活性及生命過程。量子力學把分子中的原子核看成是一個骨架,外圍電子則在這一骨架附近運動。電子不僅具有粒子性,同時還具有波動性。因此對電子的運動可以用一個波函數來描述。這個波函數應滿足量子力學中的基本方程,即薛定諤方程:
H
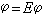 (1)
式中H稱為哈密頓算符,
E是整個體系的能量。在量子生物學中所處理的系統一般都比較復雜,但重要的生物分子常具有由π電子所組成的雙鍵,這種π電子的活動性較大,實際上並不定位在特定的一個原子核附近,這類系統稱為共軛系統。核酸中的嘌呤與嘧啶堿基、蛋白質中的芳香氨基酸、高能磷酸物、喋呤、卟啉、醌、類胡蘿卜素、各種輔酶、膽固醇以及許多藥物無不具有共軛系統。各種生命現象都和共軛系統的存在及其π電子的非定域化密切相關。因此量子生物學首先考慮瞭這類電子的運動。目前最廣泛應用的計算方法稱為分子軌道法(簡稱MO)。即認為每個電子的運動可擴及到整個分子范圍內。雖然每個電子的軌道是一種分子軌道,但它畢竟和原子軌道有關。認為分子軌道由原子軌道線性組合而成的方法就稱為原子軌道的線性組合法。簡寫為LCAO-MO法:
(1)
式中H稱為哈密頓算符,
E是整個體系的能量。在量子生物學中所處理的系統一般都比較復雜,但重要的生物分子常具有由π電子所組成的雙鍵,這種π電子的活動性較大,實際上並不定位在特定的一個原子核附近,這類系統稱為共軛系統。核酸中的嘌呤與嘧啶堿基、蛋白質中的芳香氨基酸、高能磷酸物、喋呤、卟啉、醌、類胡蘿卜素、各種輔酶、膽固醇以及許多藥物無不具有共軛系統。各種生命現象都和共軛系統的存在及其π電子的非定域化密切相關。因此量子生物學首先考慮瞭這類電子的運動。目前最廣泛應用的計算方法稱為分子軌道法(簡稱MO)。即認為每個電子的運動可擴及到整個分子范圍內。雖然每個電子的軌道是一種分子軌道,但它畢竟和原子軌道有關。認為分子軌道由原子軌道線性組合而成的方法就稱為原子軌道的線性組合法。簡寫為LCAO-MO法:
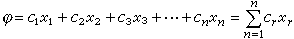 (2)
(2)
式中的x1,…,xn+1表示各原子軌道的波函數,x1,…,xn+1為相應的系數。
因此,對一個具有生物學意義的體系的量子力學計算過程,包括下列步驟:根據欲研究分子的結構,選定合適的波函數,代入波動方程(1),並求其解。然後將所得結果和欲研究的生物學活性相聯系。由於精確求解常有困難,因此在計算中經常應用各種近似方法。這種近似性是否適用,還要和實驗結果相印證。從計算結果可以得到兩類不同性質的指數:能量指數與結構指數。能量指數說明體系的能量狀態,例如總能量、躍遷能(不同狀態之間的能量差)。最高填滿分子軌道(即電離勢,簡寫作HOMO)與最低空分子軌道(即電子親合勢,簡寫為LEMO)等。結構指數說明分子的結構特征,例如鍵級(雙鍵性的大小)、自由價(通過某一原子參與化學反應的能力)、電子電荷等。
研究內容 隻要生物分子本身的化學結構或各級結構已經清楚,就有可能研究和這種分子相聯系的生物學活性的本質,或者它們之間的相互作用。因此量子生物學所研究的問題實際上涉及分子生物學的全部內容。例如重要生物大分子的物理性質、各級結構與功能;酶的結構與催化機制;酶與底物、酶與輔酶、抗原與抗體之間的特異作用;高能磷酸物的電子構造與能量關系;致癌物質的作用機制;藥物作用機制;活體中電子、質子與能量遷移及轉化關系等等。為瞭方便起見,可以把量子生物學的內容歸納為以下四個方面:
分子間相互作用力的研究 分子間的相互作用力主要考慮的是靜電力:包括引力與斥力。至於電磁力在生物分子中一般認為可以忽略。靜電力又分為強力與弱力兩種,所謂強弱是相對而言的,一般都以平均熱能kT值作為標準。k為玻耳茲曼常數,T為絕對溫度。由作用力所產生的相互作用能大於kT者為強力,反之為弱力。強力不僅在維持分子的基本骨架(一級結構)中起重要作用(包括離子鍵、共價鍵等),而且還與識別作用有關。弱力包括氫鍵、范德瓦耳斯力和偶極作用,它決定瞭分子的高級結構(二級、三級、四級結構),因而在維持大分子構象和功能活動中起十分重要的作用。
生物分子的電子結構與反應活性的研究 這是60年代前後量子生物學的主要研究領域。以核酸為例,核酸中的5種堿基都是共軛系統,由於結構不同,對輻射的抗性也不同。一般來說,嘌呤的抗性大於嘧啶;同為嘌呤,腺嘌呤又大於鳥嘌呤。按抗性大小可排列成下列次序:
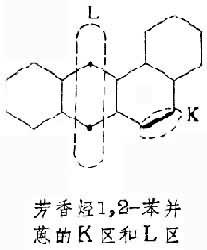
A>G>C>U>T量子生物學計算表明,這5種堿基的每個π電子的共振能的大小(能量指標之一,說明體系的穩定程度)正好符合上述次序。又如3環以上、7環以下的許多芳香烴,其中有不少有致癌活性;能致癌的烴中,其活性又有強弱不同。為瞭從理論上說明這一問題,普爾曼等提出瞭K區理論。圖中畫出瞭一個芳香烴1,2-苯並蒽的K區和一個L區。K區是進行鍵反應的部位,L區是進行對位加成反應的部位(見圖)。他們認為,致癌烴應具有化學反應能力強的K區,而L區則應較弱。他們計算瞭幾十種芳香烴,並分別用復合指標(包括鍵本身以及鍵所涉及碳原子的電子指數和能量指數)說明有無致癌活性及其強弱的判據。結果雖然還不十分滿意,但基本上為致癌活性與電子結構關系提出瞭理論依據。但應指出,對孤立分子結構的研究隻是一個方面,隻有深入研究分子與其作用對象相互作用時的結構改變,才能得到更為滿意的結果。
生物大分子的構象與功能的研究 蛋白質與核酸的空間結構及其在功能過程中的意義是這方面的主要研究課題。由於生物大分子涉及大量原子,在研究中遇到許多困難,所以這方面工作開展較晚。但對蛋白質和核酸都已瞭解到半導體性這一獨特性質的存在。這是由於弱力將不同的單元(例如蛋白質的多肽鏈)連結在一起而形成的。在這種情況下,π電子可以跨越不同的單元而非定域化。原來的能級即組合成為有一定寬度的能帶。許多人用不同的方法計算過能帶間隙與寬度,目前由於計算方法比較粗糙,和實際結果符合得不很理想。但對這一性質的說明及其在能量傳遞中的重要性提出瞭一定的根據。近年來,大分子處於溶液狀態下的溶劑化效應很受重視,特別是認識到水不僅作為生命物質的“介質”而存在,而且和大分子通過相互作用結合在一起,形成一個整體。量子力學計算能給出有關水合位置的確切信息(見生物水)。對於某些藥物,例如,組胺在兩種不同構象中產生不同的生理作用(分別刺激回腸與胃的分泌),也能從構象能量圖加以說明。
特異作用與識別機制的研究 生物學領域的一個重要特征是相互作用的特異性。藥物能和細胞表面的特異受體相互作用。一個抗體分子可以從105個分子中識別出能與之結合而起反應的抗原分子。對於這種特異作用的機制過去隻從分子大小、形狀和能否密切配合的所謂“鎖與鑰”的關系去理解。顯然,這種單純“形態學”的觀點還必需進一步從“功能”的角度加以深化,也就是研究特異作用力及其引起的構象變化。這方面工作目前不多,有待發展。但對許多生命現象的闡明(酶作用、免疫作用、藥物作用等)顯然具有關鍵性的作用。
量子生物學還是一門十分年輕的學科,國際量子生物學會(簡稱ISQB)於1970年成立。它的發展不僅需要電子計算機的協助和計算方法的改進,還需要與實驗結果密切配合。到目前為止,量子生物學還隻限於對較小分子的研究,特別是藥物的作用。對於復雜生物學問題的探討,還有待深入。
參考書目
陶宗晉等譯:《量子生物學入門》,上海科學技術出版社,1979。