幾個原子軌道經過再分配組成的互相等同的軌道。為瞭闡明共價分子的空間結構,1931年,L.鮑林在電子配對假說的基礎上,提出瞭雜化軌道理論。該理論認為:在同一個原子中能量相近的不同類型的幾個原子軌道(即波函數)可以相互疊加,而重新組成同等數量的能量完全相同的雜化原子軌道。例如,當一個碳原子和4個氫原子結合生成甲烷CH4分子時,碳原子的1個2s軌道和3個2p軌道重新組合成4個能量相等的
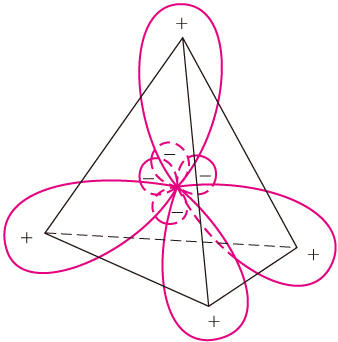 CH4分子的空間模型
CH4分子的空間模型
幾種重要的雜化軌道類型見表。
重要的雜化類型| 雜化軌道數 | 雜化類型 | 形狀 |
|---|---|---|
| 2 | sp | 直線形 |
| dp | 直線形 | sd |
| 曲線形 | 3 | sp2 |
| 平面三角形 | dp2 | 平面三角形 |
| d2s | 平面三角形 | d2p |
| 三角錐 | 4 | sp3 |
| 四面體 | d3s | 四面體 |
| dsp2 | 平面四邊形 | 5 |
| dsp3 | 三角雙錐 | d3sp |
| 三角雙錐 | d4s | 四方錐 |
| 6 | d2sp3 | 八面體 |
| d4sp | 三棱柱 |